به طوری که در معادله
زیر مشاهده می�کنید، سرعت مهاجرت یک یون υ، به قدرت
میدان الکتریکی بستگی دارد. میدان الکتریکی به نوبه
خود به وسیله�ی بزرگی پتانسیل اعمال شده (V بر حسب ولت)
و طول مسیری(L) که میدان در آن اعمال می�شود تعیین
می�گردد. بنابراین:
V/L υ= �e
این رابطه نشان می�دهد
که برای به دست آوردن مهاجرت یونی و جداسازی سریع،
پتانسیل�های اعمال شده�ی بزرگتر مطلوب هستند. بهتر است
جداسازی�های سریعتری داشته باشیم ، ولی مهمتر این است
که جداسازی�های با تفکیک بالا بدست آوریم. بنابراین
لازم است عواملی را بررسی کنیم که تفکیک در الکتروفورز
را تعیین می�کنند.
در کروماتوگرافی هم نفوذ
طولی و هم مقاومت انتقال جرم در پهن شدگی نوار مشارکت
می�کنند. با وجود این از آنجا که تنها یک فاز در
الکتروفورز درگیر است فقط نفوذ طولی را باید در نظر
گرفت. تعداد بشقابک (N) در الکتروفورز با رابطه زیر به
دست می�آید.
N= �eV/2D
که در آن D ضریب نفوذ حل
شده بر حسب cm2s-1 است. از آنجا که قدرت تفکیک با
افزایش تعداد بشقابک زیاد می�شود، بهتر است
پتانسیل�های اعمال شده�ی بالایی به کار برده شود. باید
توجه داشت که در الکتروفورز مویین همانند کروماتوگرافی،
تعداد بشقابک�ها با افزایش طول ستون زیاد نمی�شود.
طول بلند و سطح مقطع
کوچک لوله�ی مویین باعث بالا بودن مقاومت آن می�شود.
از آنجا که اتلاف توان با مقاومت نسبت عکس دارد، لذا
می�توان پتانسیل�های نسبتاً زیادتری را نیز به کار برد.
علاوه بر این، نسبت سطح به حجم زیاد لوله�ی مویین،
سرمایش کافی را در مقابل گرمایش ژول تامین می�کند. در
نتیجه�ی این دو عامل، پهن شدگی نوار در اثر اختلاط
همرفت رانده شده�ی گرمایی به میزان قابل توجهی کاهش
پیدا می�کند. لذا به راحتی می�توان پتانسیل�های تا 30
کیلو ولت را نیز به کار برد و این باعث بهبود در سرعت
و تفکیک می�شود. تعداد بشقابک�ها در الکتروفورز مویین
تا 200000 هم می�رسد، در حالی��که در HPLC این تعداد
کمتر از 20000 می�باشد.
جریان الکترواسمزی[1]
(EOF)
جریان توده�ی محلول در
لوله�ی مویین (جریان الکترواسمزی) پدیده�ای مهم در
الکتروفورز می�باشد. در الکتروفورز مویین از یک لوله�ی
سیلیکای مذاب استفاده می�شود. سطح داخلی لوله�ی مویین
که در طول آنالیز در تماس با محلول قرار می�گیرد،
دارای گروه�های سیلانول قابل یونیزه شدن می�باشد. در
محدوده�ای از pH که در الکتروفورز مویین به طور معمول
مورد استفاده قرار می�گیرد (pH بین 2 تا 9) گروه�های
سیلانول تفکیک شده و دیواره�ی داخلی دارای بار منفی
می�گردد. حال دیواره�ی باردار شده�ی منفی، یون�های
دارای بار مثبت الکترولیت را جذب کرده و یک لایه�ی
دوگانه�ی الکتریکی ایجاد می�گردد (شکل 1). با اعمال
پتانسیل مستقیم کاتیون�ها به سمت کاتد مهاجرت کرده و
توده�ی محلول اطراف را با خود حمل می�کند که نتیجه�ی
این امر ایجاد جریان الکترواسمزی به سمت کاتد می�باشد.
با برقراري ولتاژ قوي در
طول لولهی مويين، جريان الکترواسمزي ايجاد خواهد شد.
از طرفي يونها و ذرات باردار نيز به طور ذاتي داراي
حرکت الکتروفورتيک[2]
خواهند بود. برآيند اين دو حرکت براي يونها به صورت
زير است:
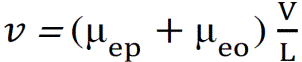
معمولاً جريان
الکترواسمزي بيشتر از تحرک الکتروفورتيک ميباشد و بر
آن غلبه دارد. نتيجهی اين امر، حرکت تمام يونها (چه
مثبت و چه منفي) و ذرات خنثي در طول لولهی مويين از
قطب مثبت به سمت قطب منفي خواهد بود. برآيند حرکت براي
يونهاي مثبت و منفي و ذرات خنثي به اين صورت خواهد
بود که ذرات با بار مثبت بيشترين سرعت مهاجرت و ذرات
با بار منفي کمترين سرعت مهاجرت را دارند. ذرات خنثي
همراه با جريان الکترواسمزي به سمت قطب منفي کشيده
ميشوند و سرعت مهاجرت آنها برابر با سرعت جريان
الکترواسمزي است. همچنين يونهاي مثبت که نسبت بار به
جرم (يا بار به شعاع يون) در آنها بزرگتر است، سريعتر
از يونهاي مثبت با نسبت بار به جرم کوچکتر مهاجرت
خواهند نمود (شکل 2)
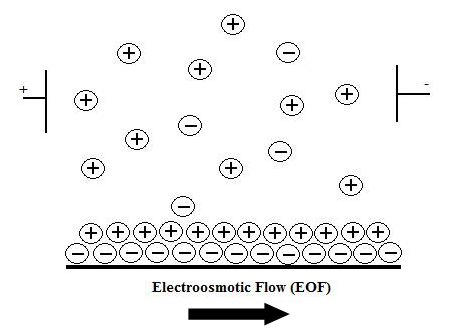
شکل 1- توزیع بار در سطح
مشترک سیلیس / مویین و جریان الکترواسمزی حاصل.
در نتیجه افزایش ولتاژ
منجر به آثار زیر می�گردد:
- افزایش جریان
الکترواسمزی
- افزایش سرعت مهاجرت
- زمان�های مهاجرت
کوتاه�تر
البته استفاده از ولتاژ
بالا می�تواند سبب ایجاد جریان الکتریکی بالا و یا
دمای بالا گردد که این عوامل می�توانند منجر به
تجزیه�ی الکترولیت زمینه / آنالیت گردند.
[2]
Electrophoretic mobility